大阪大学基礎工学研究科機能創成専攻機能デザイン領域 川野研究室
ナノ流路内におけるDNA一分子観察
DNAは塩基対のπスタッキングを介した電気伝導性や自己集合化機能を有し,生体との親和性も高く,大量合成が可能であるため,生体電子デバイスとしての利用が期待されています. 我々はDNAによる電子デバイスの創製や次世代DNAシーケンサの開発を目的としてDNA流動シミュレーション技術の確立やDNA流動の詳細解明を目指しています.
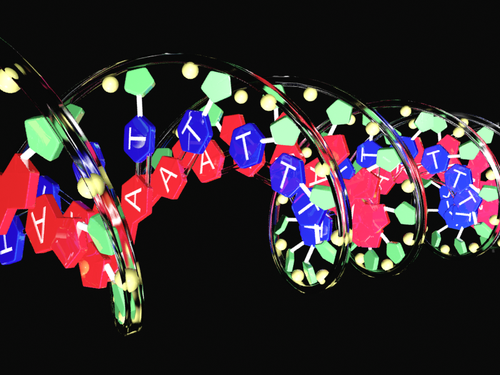
図1 poly(dA)•poly(dT)の二重らせん構造
水溶液中のDNAはその周囲に水分子の衣(水和構造)をまといながら流動すると考えられています(図2). 特に,相補的な塩基対の結合が切れたところに水分子が集中し,DNA断片の流動性に影響を及ぼすことが予想されます. このことから,一塩基多型の識別可能性が分子シミュレーションによって示唆されます.[1]
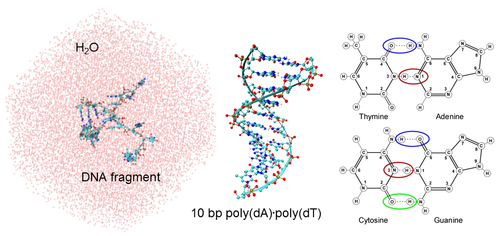
図2 水中の10塩基対DNA断片と相補的塩基対
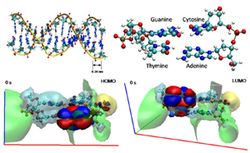
DNAは電気伝導性を示すと言われていますが,電荷の伝導メカニズムについては,未だ完全には解明されていません. 我々は,原子・電子の視点からDNA内部の電荷移動メカニズムの解明に向けた研究を行っています. 例えばB型DNAは,塩基対が重なり合った二重らせん構造を持ちます. そのような分子構造の中に分布する電子が,電場や分子振動の影響を受けることにより移動すると考えられています. 図3に示すように,グアニン(G),アデニン(A),シトシン(C),チミン(T)からなる二塩基対の電荷分布を量子力学的に計算すると,各エネルギー準位の電子波動関数(赤と青の分布)が可視化されます.さらに,定常状態にある電子波動関数について,外乱に対する応答の時間発展を計算することにより,電子の流れを見ることができます(図4). このような,解析手法の確立と実験による計測技術の発展により,DNAの電気伝導性が解明されることが期待されます.[2]
 |
 |
図3 二塩基対の電荷分布と静電ポテンシャル面 |
図4 電子波動関数の伝播 |
DNAは水溶液中で負電荷を持つことから,その泳動を電気的に制御することが可能です. 図5のように,微小電極間にDNAを誘導して電流電圧特性を調べることにより,一塩基分子を拘束に識別する技術が開発されています. 我々は,そのような系に関して,量子力学に基づいた電荷移動メカニズムを理論的に調べています.[3]
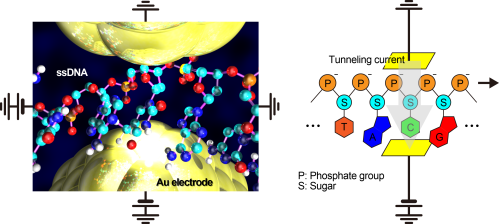
図5 金電極間にDNAを捕捉してトンネル電流により一塩基分子を識別[3]
[1] Kentaro DOI, Takamasa UEMURA, and Satoyuki KAWANO, Molecular Dynamics Study of Solvation Effect on Diffusivity Changes of DNA Fragments, Journal of Molecular Modeling, Vol. 17, No. 6 (2011), pp. 1457-1465.
[2] Kentaro DOI, Toru YONEBAYASHI, and Satoyuki KAWANO, Perturbation Theory Analysis for Electronic Response of DNA Base Pairs, J. Mol. Struct.: THEOCHEM, Vol. 939 (2010), pp. 97-105.
[3] Pawel SZAREK, Sawanya SUWANNAWONG, Kentaro DOI, and Satoyuki KAWANO, Theoretical Study on Physicochemical Aspects of Single Molecular Junction: Application to the Bases of ssDNA, The Journal of Physical Chemistry C, Vol. 117 (2013), pp. 10809-10817.